يُعد علاج الكتل السرطانية بالتخثير من الأساليب العلاجية التداخلية الحديثة التي تهدف إلى تدمير الخلايا السرطانية بشكل موضعي ودقيق، دون الحاجة إلى تدخل جراحي مفتوح. يعتمد هذا النهج على تقنيات متعددة، أبرزها التخثير الحراري باستخدام الحرارة أو البرودة، إضافةً إلى تقنيات أخرى تعمل على قطع التروية الدموية عن الورم.
يتم الإجراء عبر إدخال إبر أو مجسّات دقيقة مباشرة إلى داخل الكتلة الورمية تحت توجيه وسائل التصوير الطبي المتقدمة، مثل التصوير المقطعي أو الموجات فوق الصوتية، مما يسمح باستهداف الورم بدقة عالية مع الحفاظ على الأنسجة السليمة المحيطة. وقد أثبتت هذه التقنيات فعاليتها في علاج العديد من الأورام الصلبة، خاصة لدى المرضى غير المؤهلين للجراحة أو كجزء من خطة علاجية تكاملية تهدف إلى السيطرة على نمو الورم وتحسين جودة الحياة.
ما هو علاج الكتل السرطانية بالتخثير؟
علاج الكتل السرطانية بالتخثير هو مصطلح شامل يضم مجموعة من الإجراءات التداخلية التي تهدف إلى تدمير الورم موضعيًا أو تعطيل نموه، ويتم ذلك إما عبر تخريب الخلايا السرطانية مباشرة باستخدام الحرارة أو البرودة، أو عبر قطع التروية الدموية عن الورم من خلال الانصمام الانتقائي للأوعية المغذية له.
يُستخدم هذا النوع من العلاج بشكل شائع في سرطانات الكبد والكلى والرئة وبعض الأورام النقيلية، خاصة عندما تكون الجراحة غير ممكنة بسبب موقع الورم، حجمه، تعدده، أو بسبب الحالة الصحية العامة للمريض. ويمكن استخدام التخثير كعلاج منفرد أو بالاشتراك مع العلاج الكيميائي أو الإشعاعي ضمن خطط علاجية متكاملة.
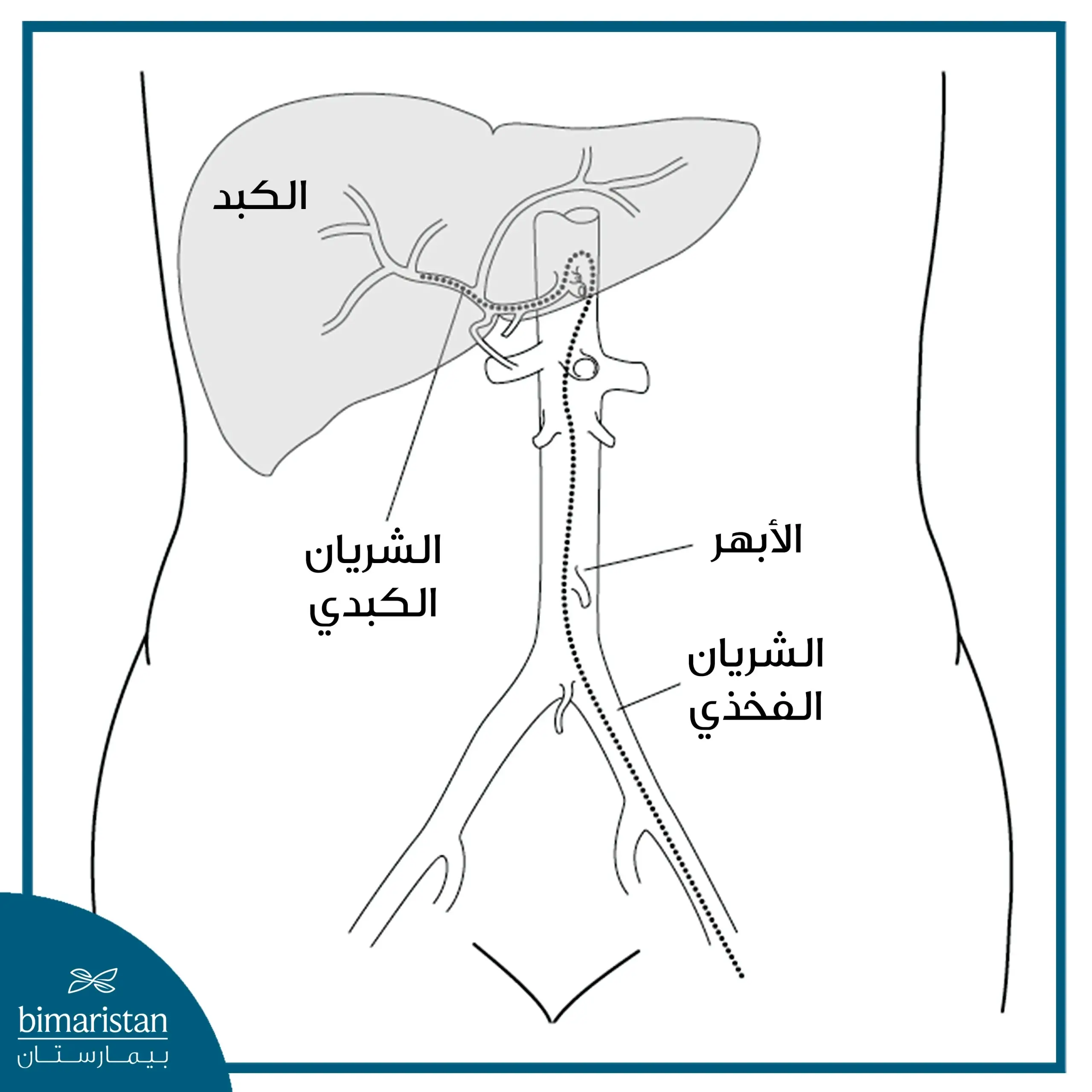
يُجرى التخثير عبر قسطرة دقيقة يتم إدخالها إلى أحد الشرايين وتوجيهها بدقة نحو الشريان المغذي للورم باستخدام تقنيات التصوير الطبي مثل الأشعة السينية، الموجات فوق الصوتية، أو التصوير المقطعي المحوسب. ومن خلال هذه القسطرة، يتم إيصال مواد انصمامية مباشرة إلى الأوعية المغذية للورم، وتشمل هذه المواد جسيمات دقيقة، أو لفائف معدنية، أو أدوية علاجية، وذلك لتحقيق انسداد انتقائي ودقيق مع الحفاظ قدر الإمكان على سلامة الأنسجة السليمة المحيطة.
يُعد التخثير الحراري من أكثر أشكال التخثير فعالية في علاج الكتل السرطانية، إذ يعتمد على تطبيق درجات حرارة مرتفعة مباشرة على الورم باستخدام التخثير بالترددات الراديوية (Radiofrequency Ablation) أو التخثير بالمايكروويف (Microwave Ablation). ولا تقتصر هذه التقنيات على سدّ الأوعية الدموية المغذية للورم فحسب، بل تؤدي أيضًا إلى تدمير الخلايا السرطانية بشكل مباشر عبر التأثير الحراري، ما يعزز من فعالية العلاج ويحدّ من نمو الورم أو يؤدي إلى انكماشه.
أنواع التخثير
يضم علاج الكتل السرطانية بالتخثير عدة تقنيات تداخلية تختلف في آلية عملها وطريقة تأثيرها على الورم، ويتم اختيار التقنية المناسبة بناءً على نوع الورم، حجمه، موقعه، ومرحلة المرض، إضافة إلى الحالة الصحية العامة للمريض. ويمكن تصنيف تقنيات التخثير المستخدمة في علاج الأورام إلى ثلاثة أنواع رئيسية:
أولًا: التخثير الحراري
يعتمد التخثير الحراري على تدمير الخلايا السرطانية بشكل مباشر عبر تعريضها لدرجات حرارة مرتفعة أو منخفضة جدًا، مما يؤدي إلى موت الخلايا الورمية. وتشمل هذه الفئة:
- التخثير بالترددات الراديوية (RFA)
- التخثير بالموجات الميكروويفية (MWA)
- التخثير بالتبريد (Cryoablation)
تُستخدم هذه التقنيات بشكل واسع في أورام الكبد والكلى والرئة وبعض الأورام العظمية، خاصةً في الحالات التي يكون فيها الورم محدود الحجم وقابلًا للاستهداف الموضعي الدقيق.
ثانيًا: التخثير غير الحراري
يمثّل التخثير غير الحراري نمطًا متقدمًا من العلاج التداخلي، وأبرز تقنياته Nanoknife (التحفيز الكهربائي غير المنعكس)، وتعتمد هذه الطريقة على إحداث خلل دائم في أغشية الخلايا السرطانية باستخدام نبضات كهربائية قصيرة وعالية الشدة، دون توليد حرارة أو برودة، مما يحافظ على سلامة البنى الحيوية المجاورة مثل الأوعية الدموية والأعصاب والقنوات الصفراوية. ويُعد هذا النوع مناسبًا بشكل خاص للأورام الواقعة في مناطق حساسة يصعب علاجها بالتخثير الحراري.
ثالثًا: التخثير الوعائي
يرتكز التخثير الوعائي على قطع التروية الدموية عن الورم عبر سدّ الشرايين المغذية له باستخدام قثاطر دقيقة، مما يؤدي إلى حرمان الخلايا السرطانية من الأكسجين والمواد المغذية. ويشمل هذا النوع:
- التخثير الكيميائي عبر الشريان (TACE)
- التخثير الشعاعي باستخدام Y-90 (TARE)
يُستخدم التخثير الوعائي بشكل أساسي في أورام الكبد البدئية والنقائل الكبدية، سواء كعلاج مستقل أو كجزء من خطة علاجية تكاملية تهدف إلى السيطرة على الورم وإبطاء تطوره.
خطوات إجراء علاج الكتل السرطانية بالتخثير
يتم علاج الكتل السرطانية بالتخثير عادة في المستشفى ويتضمن العلاج عدة خطوات رئيسية:
- يُجرى علاج الكتل السرطانية بالتخثير عادةً داخل المستشفى وفق خطوات مرتبة ودقيقة لضمان أعلى درجات الأمان والفعالية. تبدأ العملية بمرحلة التحضير، حيث يُوضَع المريض في وضعية مريحة، ويُعطى تخدير موضعي لتخدير منطقة إدخال القسطرة، مع إمكانية اللجوء إلى التخدير العام في بعض الحالات الخاصة تبعًا للحالة الصحية للمريض وتعقيد الإجراء.
- تلي ذلك مرحلة إدخال القسطرة، إذ يُجرى شق جلدي صغير—غالبًا في منطقة الفخذ—وتُدخل القسطرة إلى داخل الأوعية الدموية تحت توجيه تقنيات التصوير الطبي، ثم تُمرَّر بدقة عبر الشرايين حتى تصل إلى الأوعية المغذية للورم المستهدف.
- بعد الوصول إلى موقع الورم، تبدأ مرحلة التخثير والعلاج الحراري، حيث يتم حقن المواد الإصمامية مثل الجسيمات الدقيقة أو الملفات المعدنية أو الأدوية، بهدف قطع التروية الدموية عن الورم. وعند استخدام التخثير الحراري، تنقل القسطرة أو الإبرة الخاصة حرارة مباشرة إلى داخل الورم، ما يؤدي إلى تدمير الأنسجة السرطانية والقضاء على الخلايا الورمية.
- في المرحلة الأخيرة، وهي المراقبة بعد الإجراء، يُتابَع المريض عن كثب لرصد أي مضاعفات محتملة مثل النزيف أو الإنتان. ويتمكن معظم المرضى من مغادرة المستشفى في اليوم نفسه أو في اليوم التالي، وذلك اعتمادًا على مدى تعقيد الإجراء والحالة الصحية العامة للمريض.
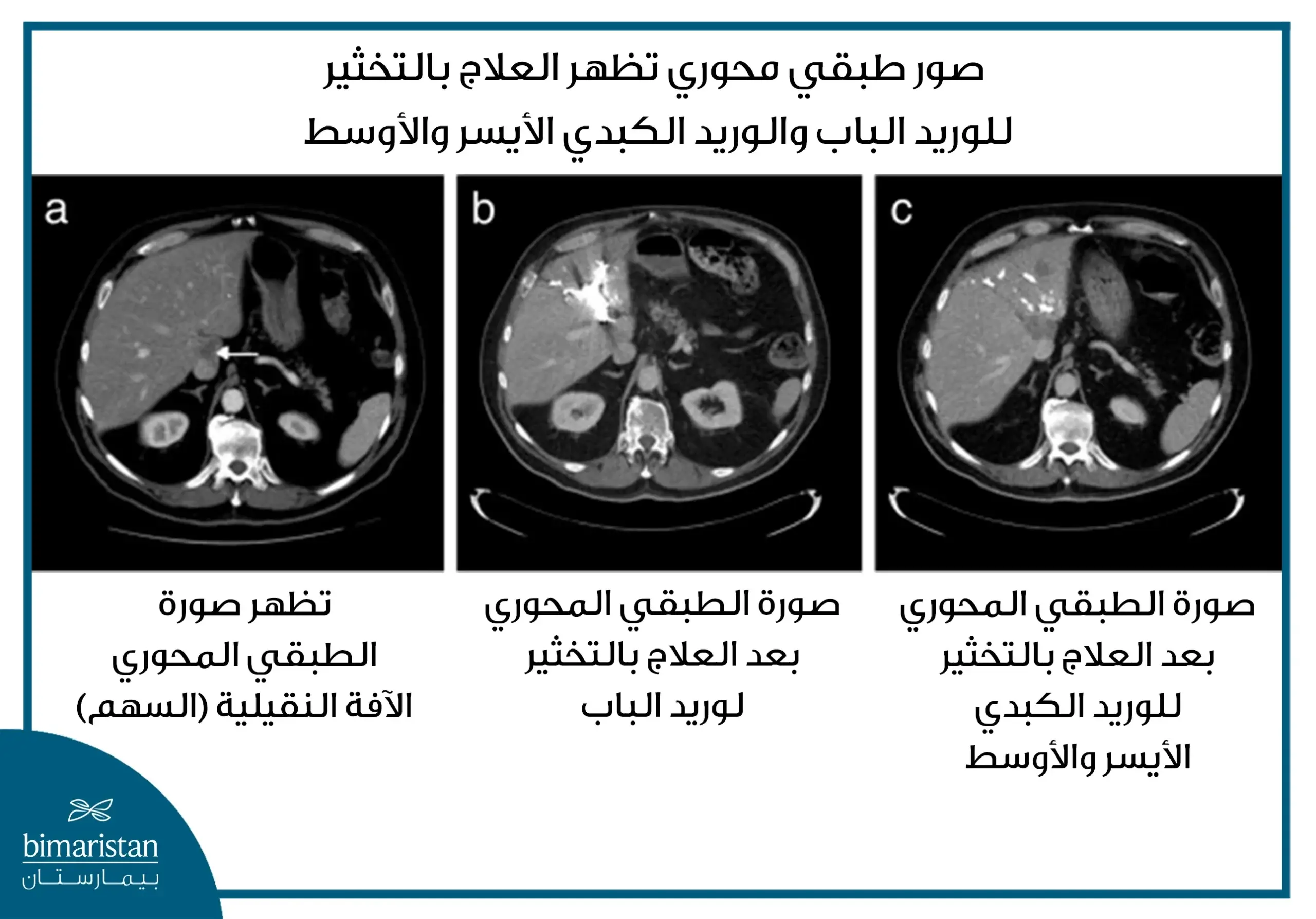
كيف تعمل تقنية التخثير الحراري على الأورام؟
يعتمد علاج الكتل السرطانية بالتخثير الحراري على آلية علاجية مزدوجة تجمع بين قطع التروية الدموية عن الورم وتطبيق الحرارة مباشرة على نسيجه، وذلك باستخدام تقنيتي الاستئصال بالترددات الراديوية (RFA) أو الاستئصال بالمايكروويف (MWA). تولّد هاتان التقنيتان درجات حرارة مرتفعة داخل الورم تؤدي إلى تخثّر الأنسجة السرطانية وتدمير الخلايا الورمية، ما قد يسبب انكماش الورم أو القضاء عليه بالكامل في بعض الحالات المختارة.
تُعد هذه التقنية خيارًا علاجيًا مهمًا للأورام التي يصعب استئصالها بالجراحة التقليدية أو علاجها بالإشعاع، ولا سيما في سرطانات الكبد والكلى، حيث قد يجعل موقع الورم أو الوضع الصحي العام للمريض التدخل الجراحي غير مناسب. ففي حالات الكتل السرطانية الكلوية مثلًا، يتولى أخصائي الأشعة التداخلية إجراء التخثير الحراري تحت تخدير ناحي أو تخدير عام بحسب طبيعة الحالة. وقد تُستخدم قسطرة بولية مؤقتة لتصريف البول من المثانة، تُزال عادة بعد فترة قصيرة من انتهاء الإجراء.
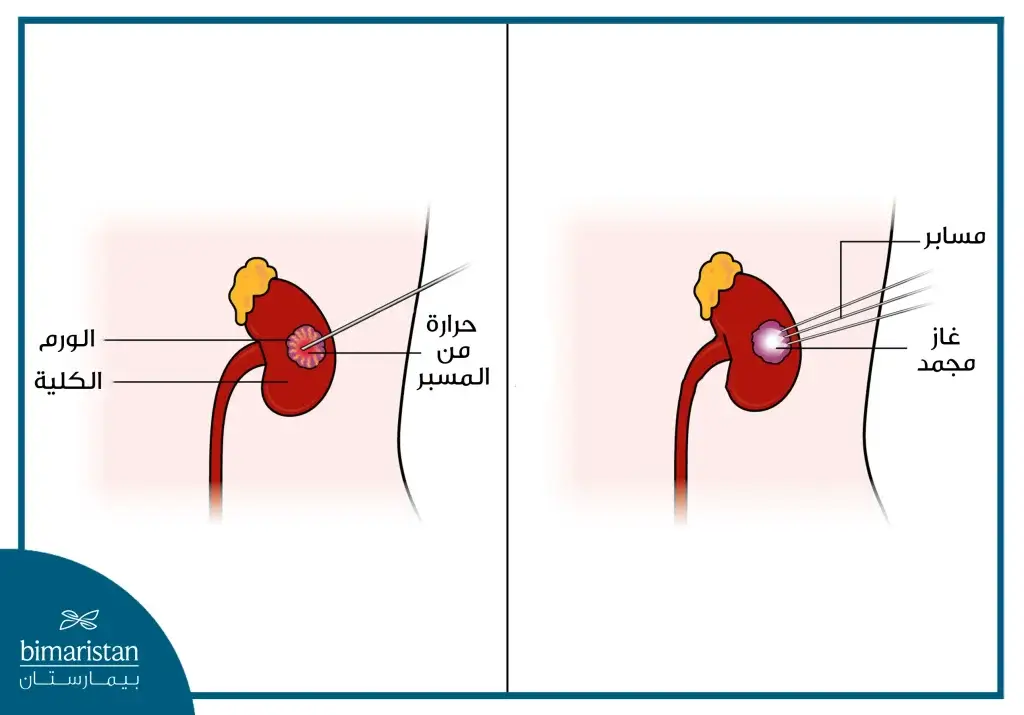
أثناء العملية، يُستخدم مخدر موضعي لتخدير المنطقة المستهدفة، ثم تُجرى فحوصات توجيهية مثل الموجات فوق الصوتية (US) أو التصوير المقطعي المحوسب (CT) لتحديد موقع الورم بدقة ومراقبة سير العلاج بشكل لحظي. وبمجرد تحديد الكتلة الورمية على شاشة التصوير، يُدخل الطبيب مسبارًا واحدًا أو أكثر عبر الجلد مباشرة إلى داخل الورم.
تعمل هذه المسابر على تسخين الورم (وأحيانًا تجميده بحسب التقنية المستخدمة)، حيث تؤدي درجات الحرارة المرتفعة إلى تدمير الخلايا السرطانية. كما يحرص الطبيب على إتلاف هامش أمان من الأنسجة السليمة المحيطة بالورم، يبلغ نحو 1 سم، بهدف تقليل احتمال بقاء خلايا سرطانية مجهرية قد تؤدي إلى عودة نمو الورم مستقبلًا. وبهذه الآلية، يوفّر التخثير الحراري علاجًا موضعيًا دقيقًا وفعّالًا مع الحفاظ على أكبر قدر ممكن من الأنسجة السليمة.
الفرق بين التخثير بالترددات الراديوية (RFA) والتخثير بالمايكروويف (MWA)
تعد كل من تقنية التخثير بالترددات الراديوية RFA والتخثير بالمايكروويف MWA تقنيات فعالة لعلاج الكتل السرطانية، حيث يعتمد اختيار الطريقة على حجم الورم وموقعه وعوامل سريرية أخرى، ويكمن الفرق بينهما:
| المعيار | التخثير بالترددات الراديوية (RFA) | التخثير بالمايكروويف (MWA) |
|---|---|---|
| آلية توليد الحرارة | يستخدم تيارات كهربائية عالية التردد | يستخدم طاقة الميكروويف |
| درجة الحرارة | يسخّن الأنسجة بشكل أبطأ | أكثر كفاءة في توليد درجات حرارة أعلى |
| سرعة العلاج | يتطلب وقت علاج أطول نسبيًا | معالجة أسرع |
| حجم الورم المناسب | مناسب للأورام الصغيرة (أقل من 3 سم) | مناسب أكثر للأورام الأكبر أو متعددة البؤر |
| التأثير على الأنسجة | تأثير موضعي محدود وأكثر دقة | تأثير أوسع مع تسخين أكثر انتظامًا |
| التأثر بتدفق الدم (Heat Sink) | يتأثر أكثر بتدفق الدم القريب من الورم | أقل تأثرًا بتدفق الدم |
| التحكم بمنطقة الاستئصال | جيد لكن محدود الحجم | أفضل في السيطرة على مناطق استئصال كبيرة |
مزايا علاج الكتل السرطانية بالتخثير مقارنةً بالجراحة
يقدم علاج الكتل السرطانية بالتخثير وخاصةً عند استخدام تقنيات التخثير الحراري للأورام مثل RFA وMWA العديد من المزايا مقارنة بالجراحة التقليدية، فهي:
- أقل تدخلاً: يتم إجراء استئصال الورم من خلال شق صغيرعلى عكس الجراحة التي تتطلب شقوقاً كبيرة (غالباً في الفخذ أو الرسغ) حيث يتم إدخال القسطرة. يؤدي هذا إلى انخفاض خطر الإصابة بالعدوى وتقليل وقت التعافي.
- ذات وقت أقصر للتعافي: عادةً ما يتعافى المرضى الذين يخضعون للاستئصال بشكل أسرع مقارنة بمن يخضعون للجراحة. غالباً ما تكون فترات الإقامة في المستشفى أقصر ويمكن للعديد من المرضى العودة إلى أنشطتهم الطبيعية في غضون أيام إلى أسبوع.
- ذات خطر أقل لحدوث مضاعفات: نظراً لأن علاج الكتل السرطانية بالتخثير أقل تدخلاً فإن خطر المضاعفات مثل العدوى والنزيف يكون أقل عموماً مقارنة بالجراحة. هناك أيضاً مخاوف أقل بشأن الندبات أو تلف الأنسجة السليمة.
- ذات إمكانية للتكرار: يمكن إجراء العلاج بالتخثير عدة مرات إذا لزم الأمر، ولكن قد لا تكون الجراحة خياراً قابلاً للتطبيق للأورام المتكررة أو المتعددة.
- ذات فعالية في الأورام غير القابلة للجراحة: بالنسبة للمرضى الذين يعانون من أورام يصعب أو يستحيل إزالتها جراحياً بسبب موقعها أو صحة المريض فإن علاج الكتل السرطانية بالتخثير يوفر بديلاً قابلاً للتطبيق وهذا شائع بشكل خاص في حالات سرطان الكبد أو سرطان الكلى مع وجود أورام بالقرب من بنى حيوية.
- إجراء مكمل لعلاجات أخرى: يمكن أيضاً استخدام التخثير بالاشتراك مع علاجات أخرى مثل التخثير الكيميائي أو التخثير الشعاعي، حيث يمكن أن يعزز هذا من فعالية العلاج بشكل عام وخاصةً في مراحل السرطان المتقدمة.
فعالية العلاج بالتخثير مقارنة بالعلاجات الأخرى
يُعد علاج الأورام بالتخثير خيارًا علاجيًا فعّالًا، لا سيما في الأورام التي يصعب التعامل معها بالجراحة التقليدية. ورغم أنه ليس علاجًا شافيًا لجميع أنواع السرطان، فإنه يقدّم فوائد كبيرة لفئات محددة من المرضى، خاصةً غير المرشحين للجراحة. وبالمقارنة مع الجراحة أو العلاج الإشعاعي أو العلاج الكيميائي، يتميّز التخثير بكونه أقل توغّلًا، مع معدلات مضاعفات أقل وفترة تعافٍ أقصر. كما يمكن دمجه ضمن خطط علاجية متعددة الوسائط لتعزيز الفعالية، ما يجعله أداة محورية في علاج أورام الكبد والكلى على وجه الخصوص.
الحالات المناسبة لعلاج أورام الكبد والكلية بالتخثير
لا يُعد التخثير مناسبًا لكل مريض أو لكل ورم، لكنه يُمثّل خيارًا فعّالًا في سيناريوهات محددة:
سرطان الكبد (سرطان الخلايا الكبدية)
غالبًا ما يُشخَّص سرطان الكبد في مراحل متقدمة، وقد تكون الجراحة غير ممكنة لدى عدد كبير من المرضى بسبب تشمّع الكبد، أو كِبر حجم الورم، أو ضعف الحالة العامة. في هذه الحالات، يُفضَّل التخثير كخيار علاجي موضعي، ويُستخدم على نطاق واسع كلٌّ من التخثير الكيميائي والتخثير الشعاعي للسيطرة على الورم وتحسين النتائج.
سرطان الكلى (سرطان الخلايا الكلوية)
رغم أن الجراحة تظل الخيار الأول، فإن التخثير يُعد بديلًا مناسبًا عندما تكون الجراحة غير ممكنة، مثل المرضى ذوي الخطورة الجراحية العالية أو المصابين بأورام متعددة. كما يفيد التخثير في السيطرة على النزيف المرتبط بالسرطان المتقدم أو في معالجة أورام يصعب الوصول إليها جراحيًا.
السرطانات النقيلية
عند انتقال السرطان إلى الكبد أو الكلى من أعضاء أخرى، يمكن للتخثير أن يُقلّص حجم النقائل ويُحسّن الأعراض. ورغم أنه لا يُعد علاجًا شافيًا، فإنه يساهم في تحسين نوعية الحياة وتخفيف العبء المرضي لدى المرضى المصابين بمرض نقائلي.
الأورام التي تنكس بعد الجراحة
في حال عودة الورم بعد الاستئصال الجراحي، يُمكن استخدام التخثير كعلاج مُساند للحد من نمو الورم أو للسيطرة على الأعراض، ريثما تتاح خيارات علاجية أخرى أو كجزء من خطة علاجية تكاملية.
بهذا، يُمثّل التخثير خيارًا مرنًا وفعّالًا ضمن منظومة علاج السرطان، خاصةً عندما تُقيّد الجراحة أو العلاجات التقليدية بحدود تقنية أو صحية.
المخاطر والتحديات في علاج السرطان بالتخثير
على الرغم من أن علاج الكتل السرطانية بالتخثير يوفر العديد من الفوائد، إلا أنه ليس خالياً من المخاطر والتحديات، حيث يتطلب هذا الإجراء الدقة، ويشمل مضاعفات محتملة منها:
- الإنتان: خاصةً في مكان إدخال القسطرة، ويمكن السيطرة عليه بالصادات الحيوية.
- خطر النزف: حدوث نزيف في العضو المستهدف أو في موقع إدخال القسطرة، حيث يتم استخدام أدوات التصوير لتجنب حدوث النزف.
- أعراض إنفلونزا بعد إجراء الاستئصال بالتخثير: بما في ذلك الحمى والألم والغثيان والتعب، وتكون هذه الأعراض مؤقتة.
- التدمير غير الكامل للورم: في حين أن التخثير يمكن أن يقلص الأورام بشكل كبير، إلا أنه قد لا يقضي دائماً على السرطان بشكل تام. في بعض الحالات، قد تكون هناك حاجة إلى علاجات إضافية مثل الجراحة أو الإشعاع أو العلاج الكيميائي.
- إمكانية حدوث النكس: حتى بعد نجاح الانسداد هناك خطر تكرار الورم، لذلك تعتبر المراقبة المستمرة ضرورية لتقييم نجاح العلاج.
الآثار الجانبية الشائعة عند التخثير الحراري للأورام
على الرغم من أن التخثير الحراري للأورام آمن بشكل عام إلا أنه قد يسبب بعض الآثار الجانبية، بما في ذلك:
- الألم وعدم الراحة: قد يعاني بعض المرضى من الألم في موقع إدخال القسطرة أو في منطقة الورم المعالج.
- الغثيان والإقياء: الغثيان بعد العملية شائع وعادة ما يهدأ في غضون أيام قليلة.
- التعب والحمى: وهي حالة تُعرف باسم متلازمة ما بعد العلاج بالتخثير post-embolization syndrome، حيث أفاد العديد من المرضى أنهم يشعرون بالتعب والحمى بعد العملية.
- العدوى أو النزيف: هناك خطر الإصابة بالعدوى أو النزيف كما هو الحال مع أي إجراء يتضمن إدخال قسطرة.
نكس الأورام بعد العلاج بالتخثير الحراري
يُعد نكس الأورام بعد العلاج بالتخثير الحراري من المضاعفات المحتملة في بعض الحالات، على الرغم من الفعالية العالية لهذه التقنية في تدمير الخلايا السرطانية باستخدام درجات حرارة مرتفعة. ففي بعض المرضى، قد يعاود الورم النمو بعد فترة من العلاج، ويعود ذلك إلى عدة عوامل، من أبرزها مقاومة بعض الخلايا السرطانية للحرارة، أو عدم شمول منطقة التخثير لكامل الكتلة الورمية وهوامش الأمان المحيطة بها، خاصة في الأورام الكبيرة أو ذات الأشكال غير المنتظمة. كما قد يلعب الموقع التشريحي للورم وقربه من أوعية دموية كبيرة دورًا في تقليل فعالية التخثير بسبب تبديد الحرارة.
لهذا السبب، تتطلب هذه الحالات متابعة دقيقة بعد الإجراء، تشمل التصوير الدوري باستخدام التصوير المقطعي المحوسب أو الرنين المغناطيسي، إضافة إلى تقييم المؤشرات السريرية والمخبرية. وفي حال اكتشاف النكس مبكرًا، يمكن اللجوء إلى جلسات تخثير إضافية أو دمج التخثير الحراري مع علاجات أخرى مثل التخثير الكيميائي أو الشعاعي أو حتى الجراحة عند الإمكان، وذلك بهدف تحسين السيطرة على المرض وتحقيق أفضل النتائج العلاجية الممكنة.
ختاماً، يمثل علاج الكتل السرطانية بالتخثير خياراً علاجياً فعالاً وآمناً في حالات مختارة، لما يوفره من دقة عالية، وقلة التوغل، وانخفاض معدلات المضاعفات مقارنة بالجراحة التقليدية. كما يساهم في تقصير فترة التعافي وتحسين جودة حياة المرضى، سواء استُخدم كعلاج أساسي أو كجزء من خطة علاجية متكاملة. ومع التطور المستمر في تقنيات التوجيه والتصوير، يزداد الاعتماد على التخثير كحل علاجي متقدم في مراكز علاج الأورام الحديثة.
المصادر:
- National Cancer Institute. (n.d.). Embolization. In NCI Dictionary of Cancer Terms. U.S. Department of Health and Human Services.
- Thacker, P. G. (2009). Embolization of nonliver visceral tumors



